根据《总局办公厅关于做好医疗器械临床试验机构备案工作的通知》中的要求,自2019年1月1日起,医疗器械(包括体外诊断试剂)临床试验申办者应当选取已经在备案系统备案的医疗器械临床试验机构,按照《医疗器械临床试验质量管理规范》(食品药品监管总局 国家卫生计生委令第25号)和《体外诊断试剂注册管理办法》(食品药品监管总局令第5号)的有关要求开展临床试验。
这就意味着元旦假期后,没有完成医疗器械临床试验机构备案的医疗机构将不能开展临床试验项目。
截止2019年1月2日——2019年第一个工作日,全国共有680家医疗机构成功完成医疗器械临床试验机构备案工作。
也有消息称目前是682家,从编号上来看,备案号械临机构备201800240号和械临机构备201800366号机构已经查询不到了,所以目前实际应该是680家机构。

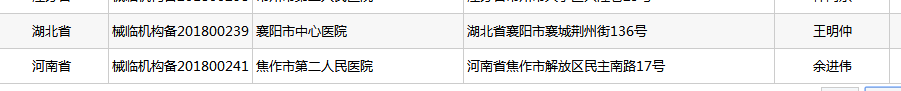
致众按照各省份汇总如下:
安徽省(13家)
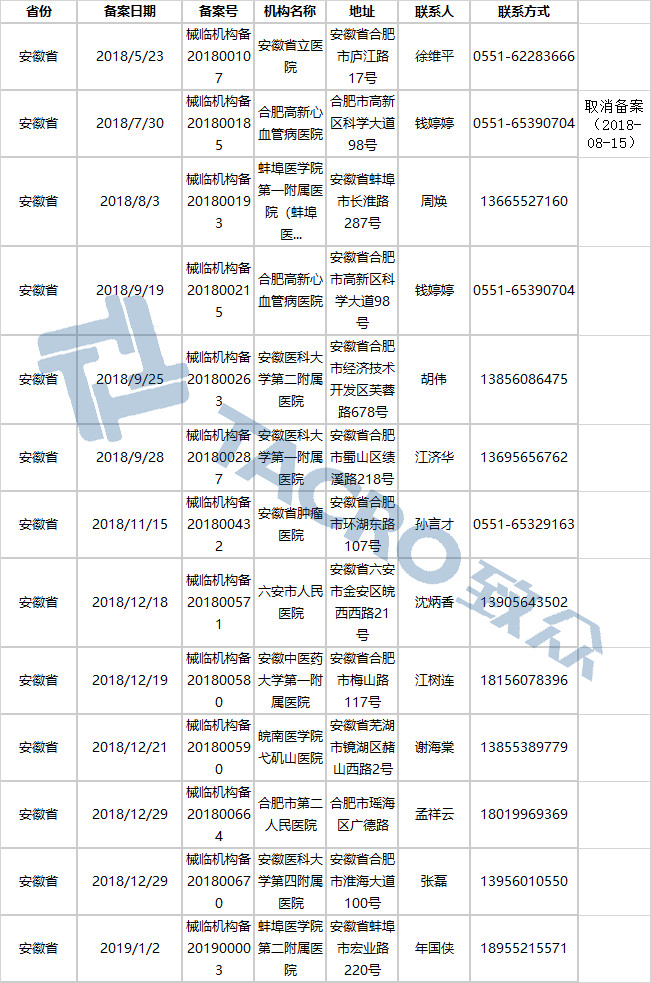
北京市(55家)
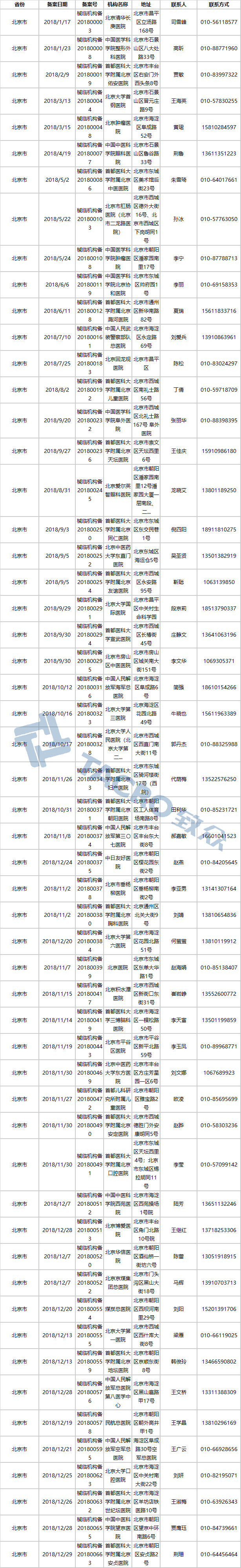
重庆市(15家)
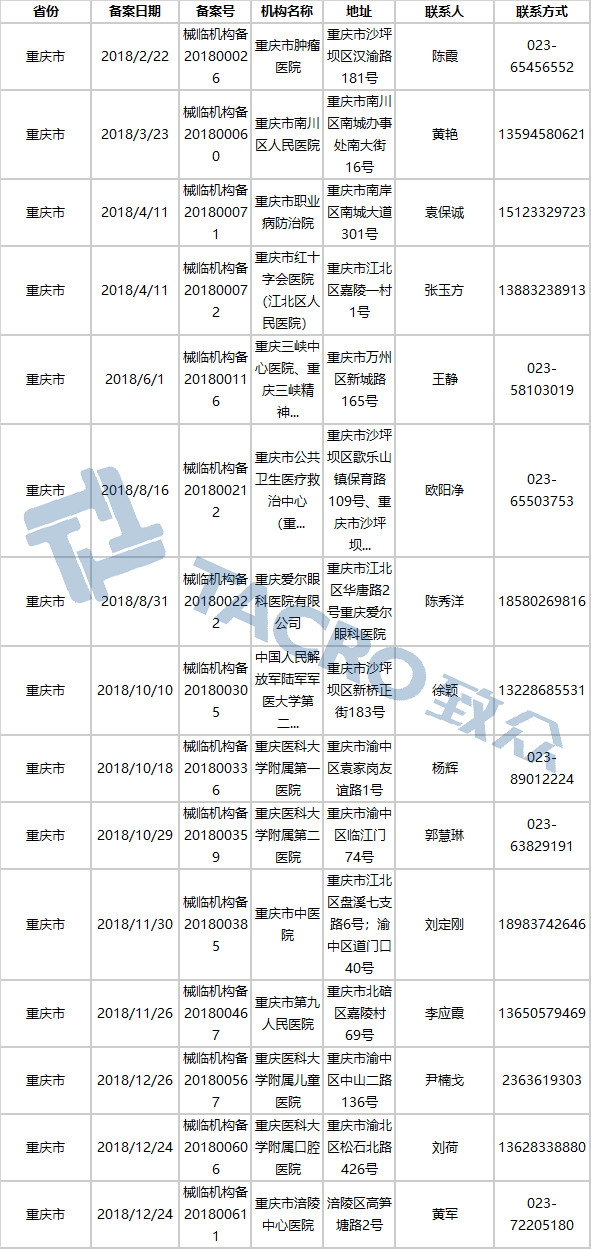
福建省(19家)

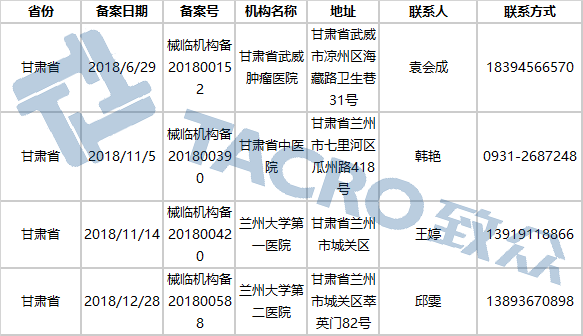
甘肃省(4家)
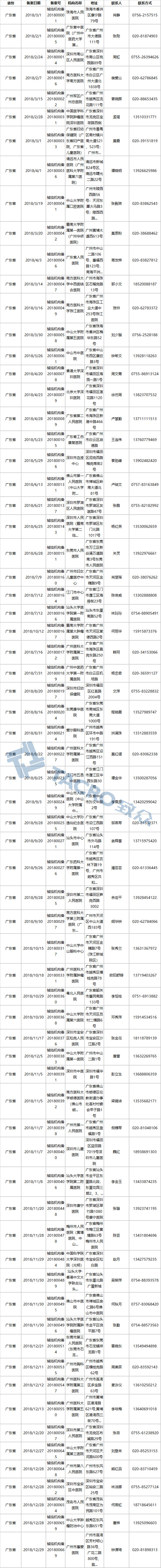
广东省(69家)
广西壮族自治区(11家)

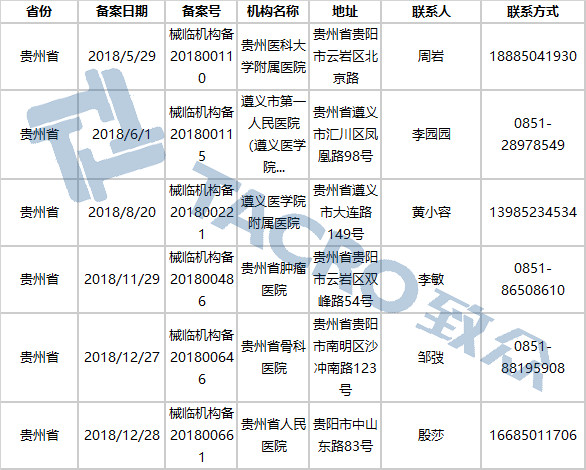
贵州省(8家)
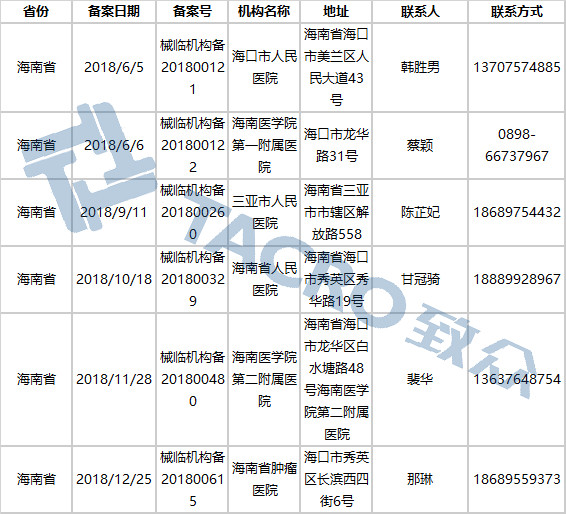
海南省(6家)
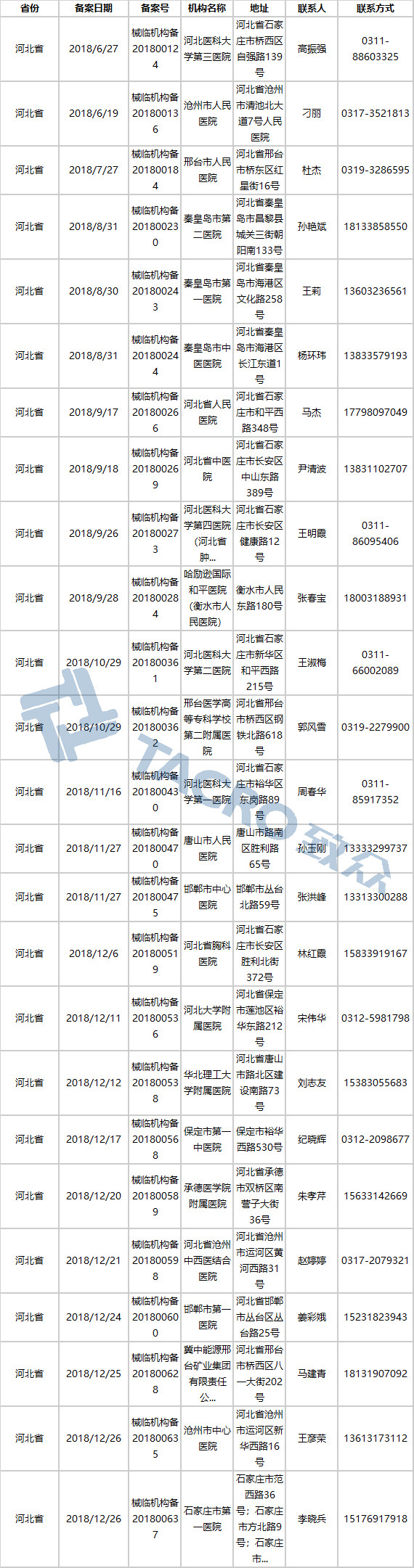
河北省(25家)
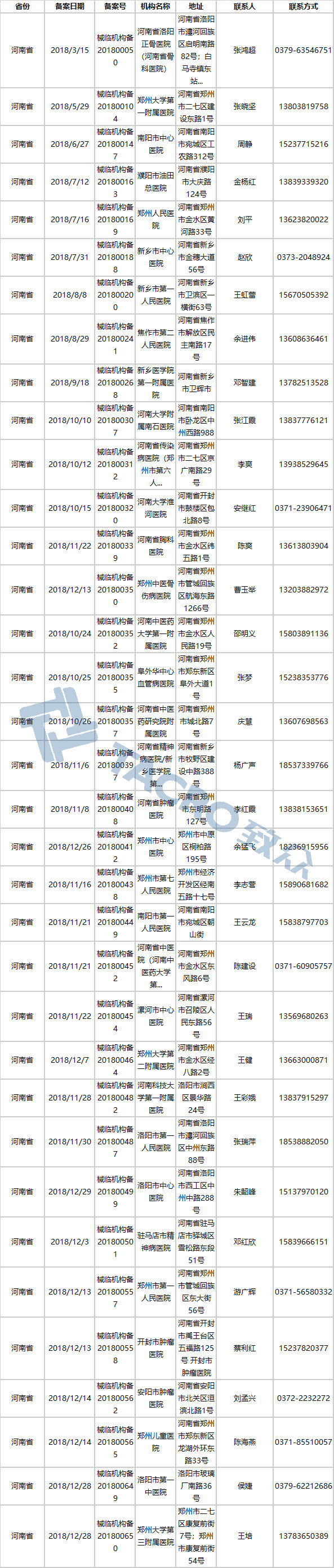
河南省(35家)
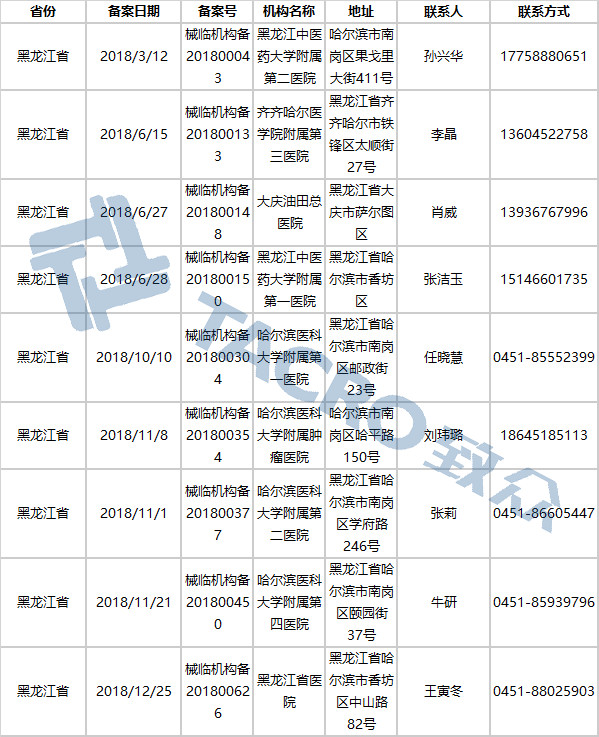
黑龙江省(9家)
湖北省(25家)

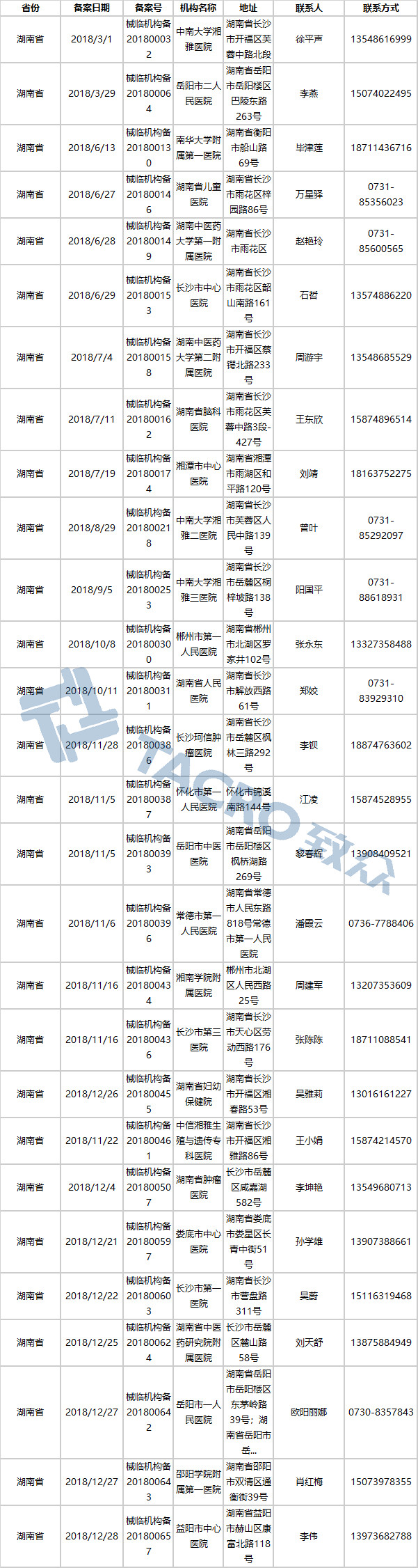
湖南省(28家)
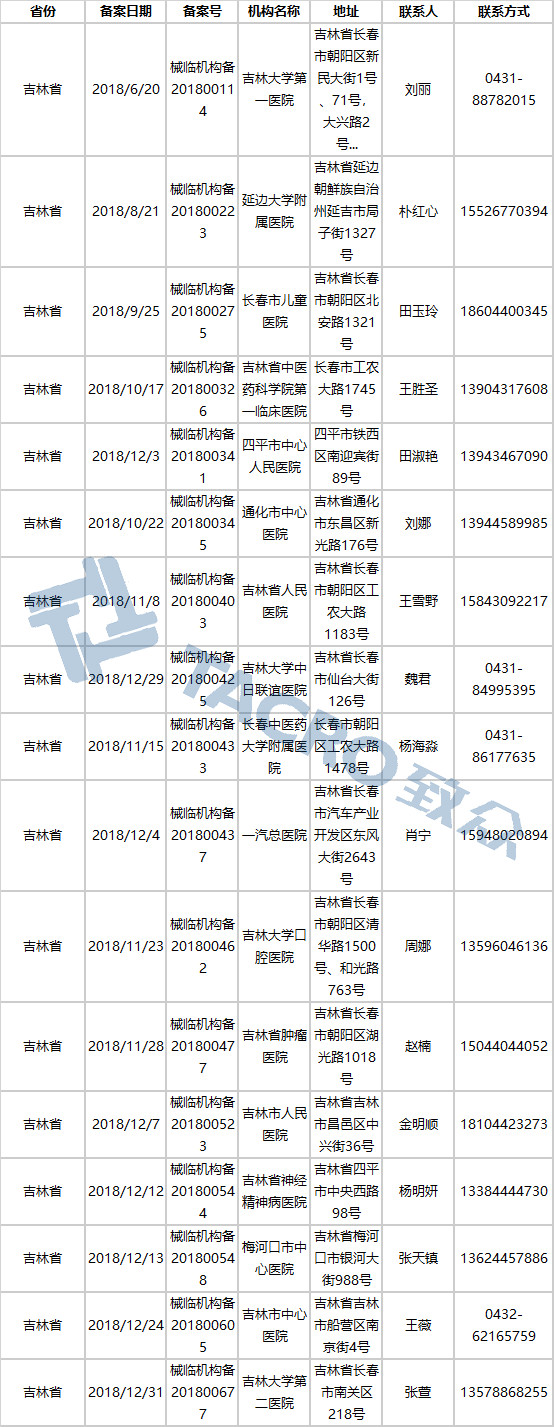
吉林省(19家)
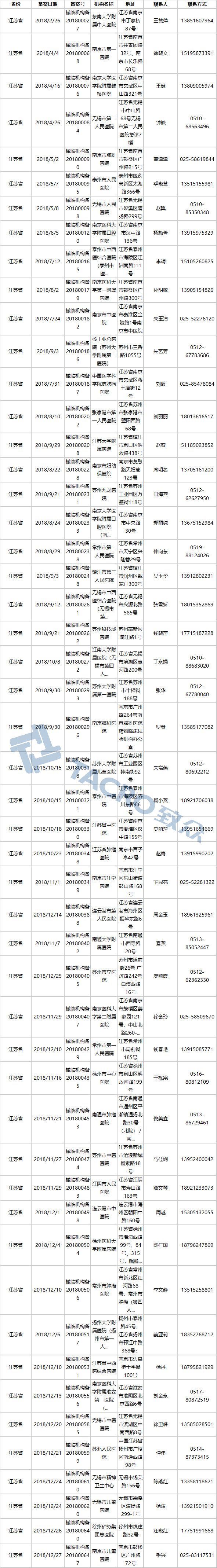
江苏省(51家)
江西省(21家)

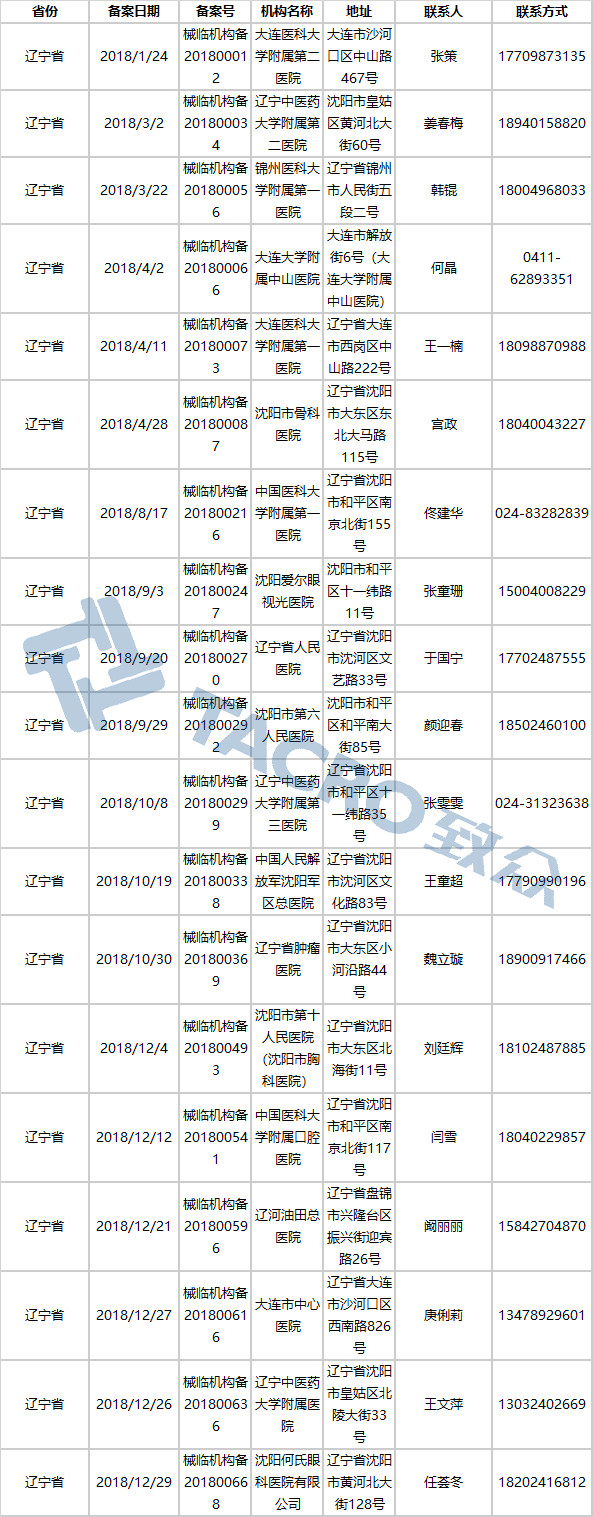
辽宁省(19家)
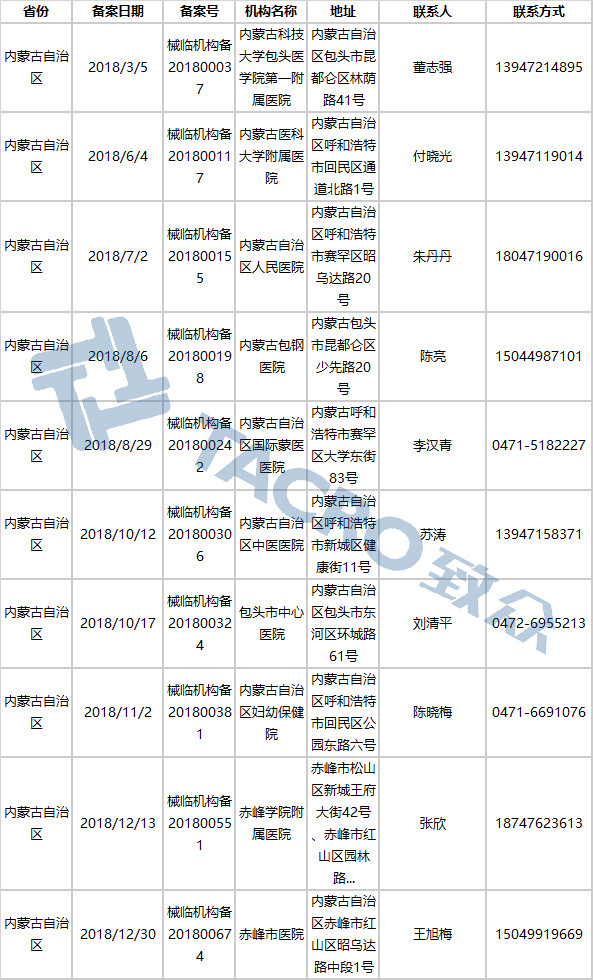
内蒙古自治区(10家)
宁夏回族自治区(4家)
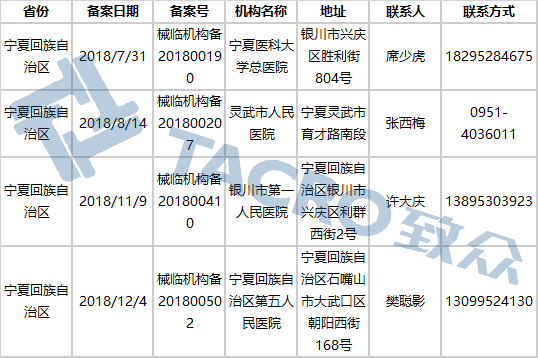
山东省(41家)
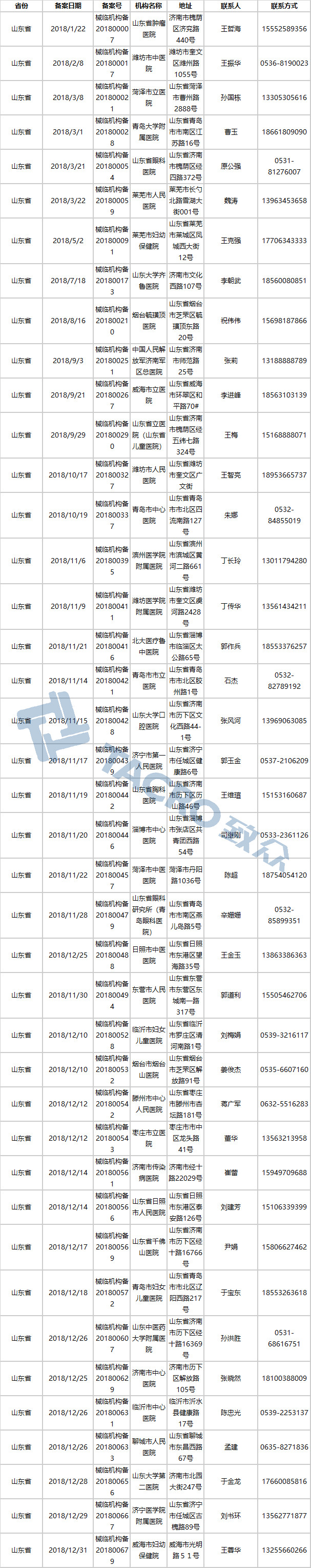
山西省(20家)
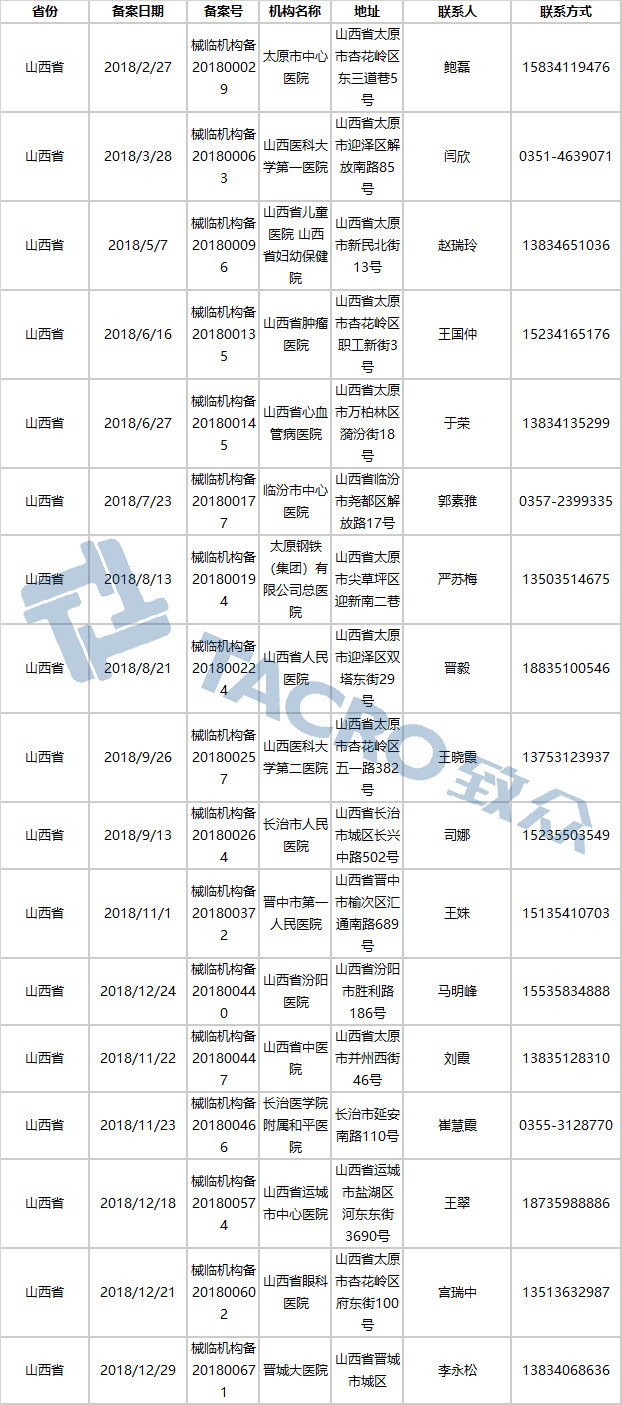
陕西省(11家)
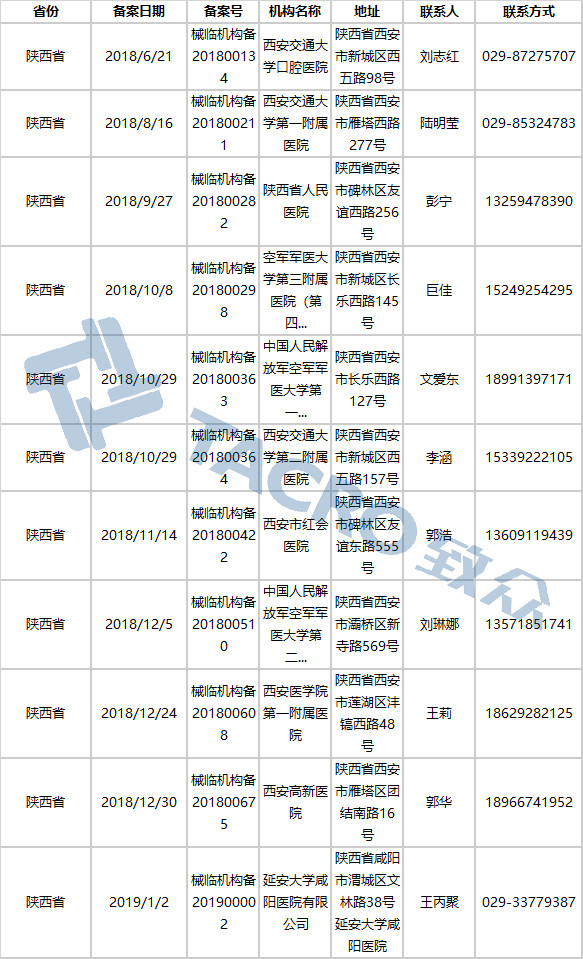
上海市(52家)
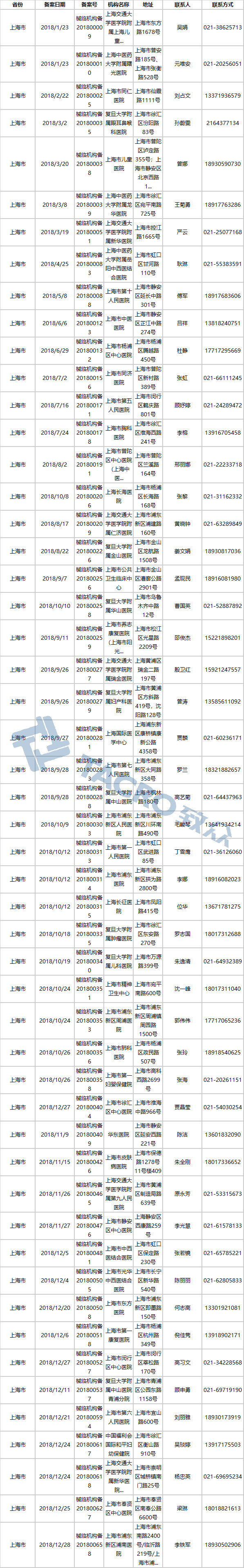
四川省(33家)
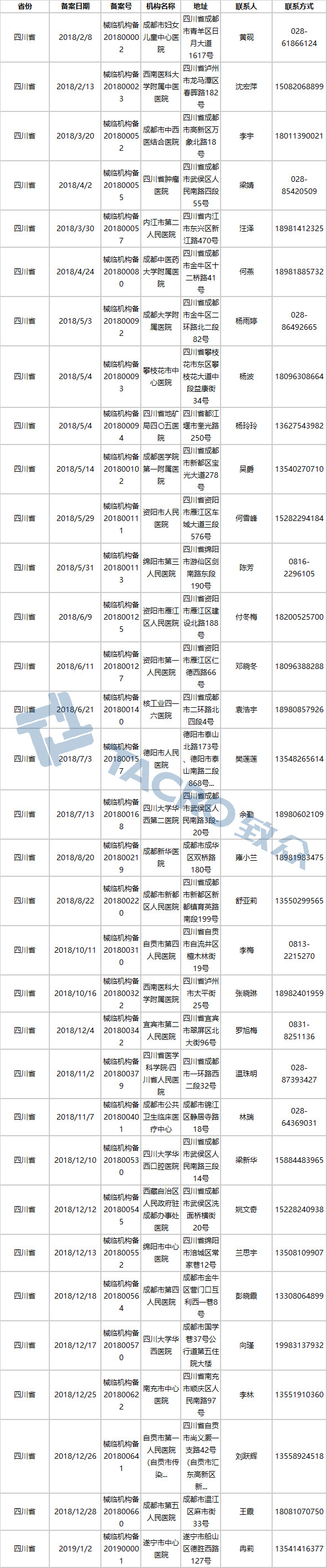
天津市(27家)
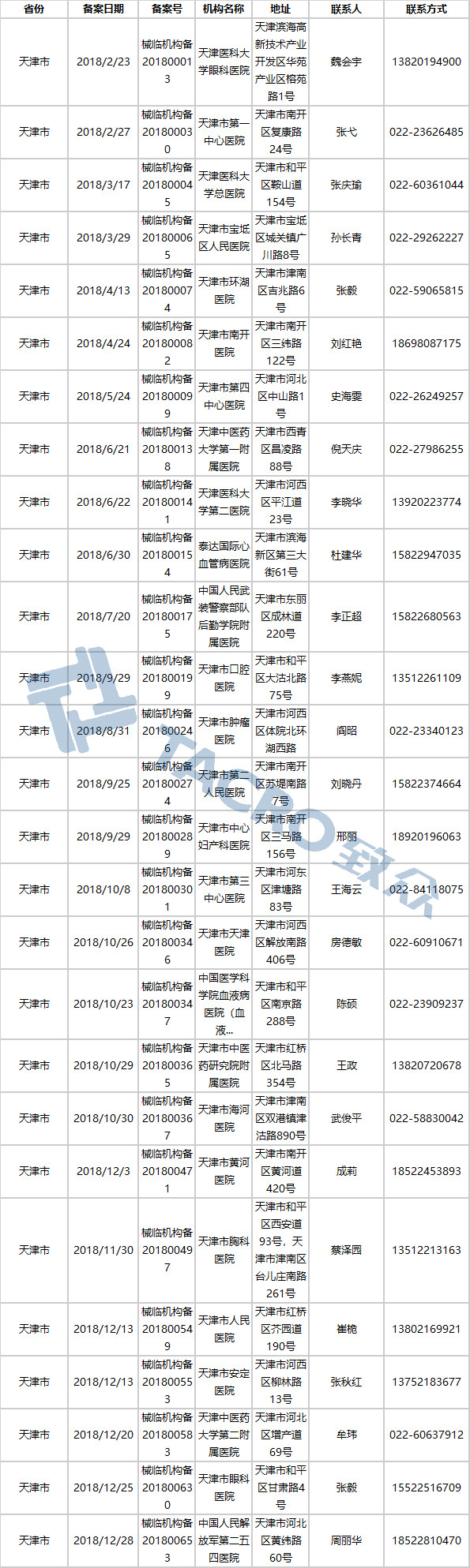
新疆维吾尔自治区(7家)

云南省(9家)
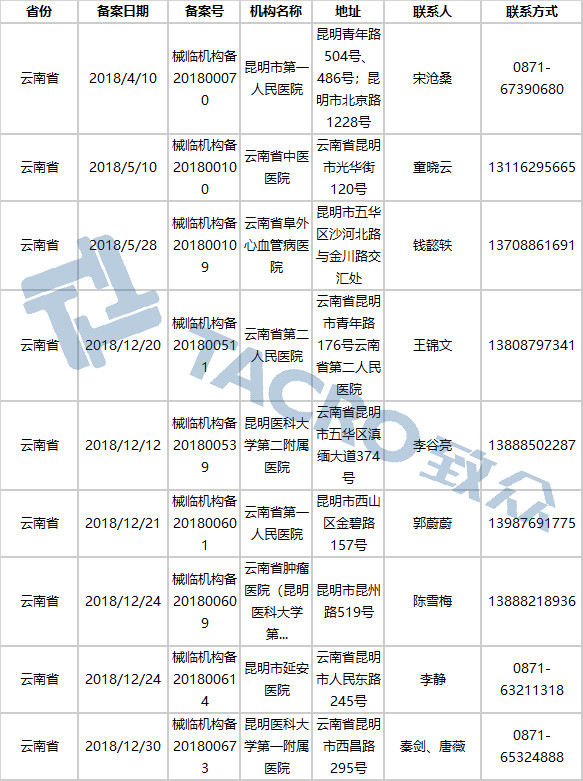
浙江省(40家)
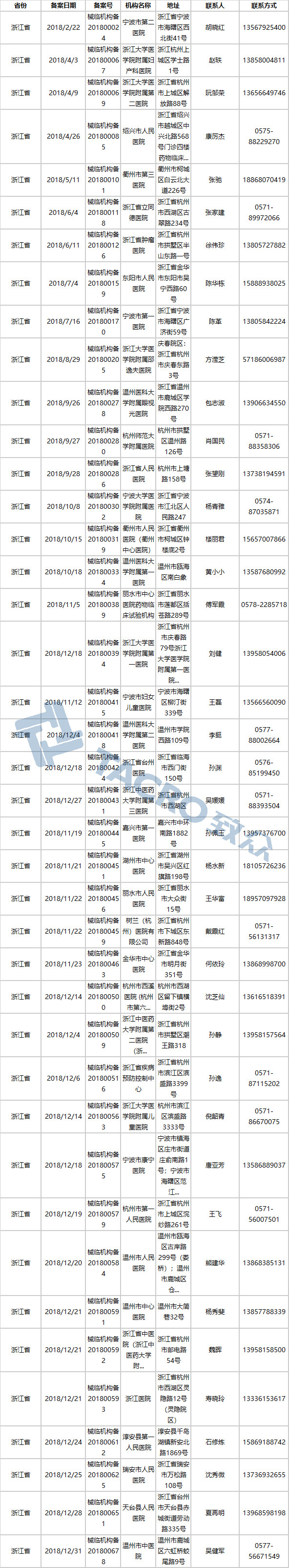
来源: NMPA