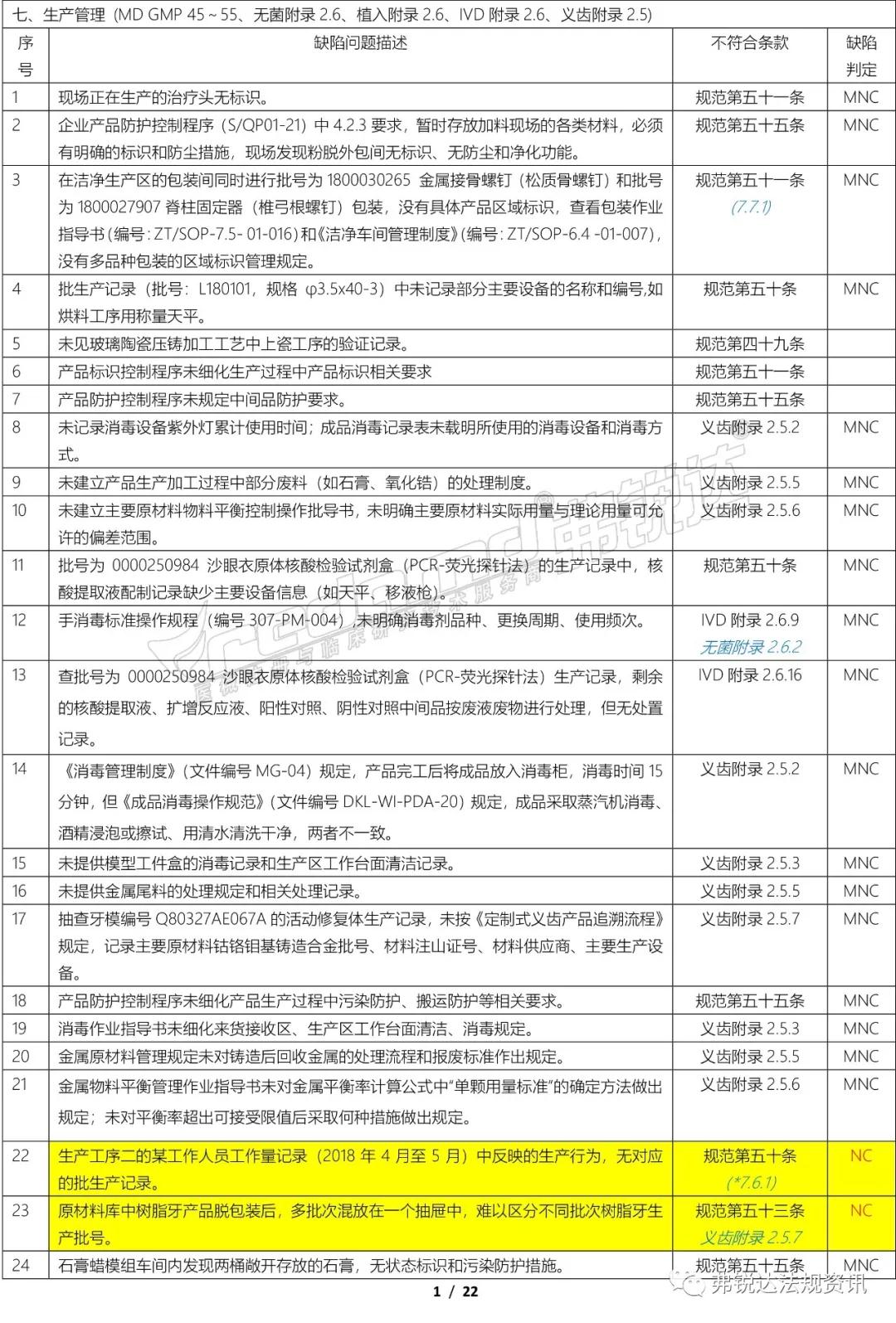
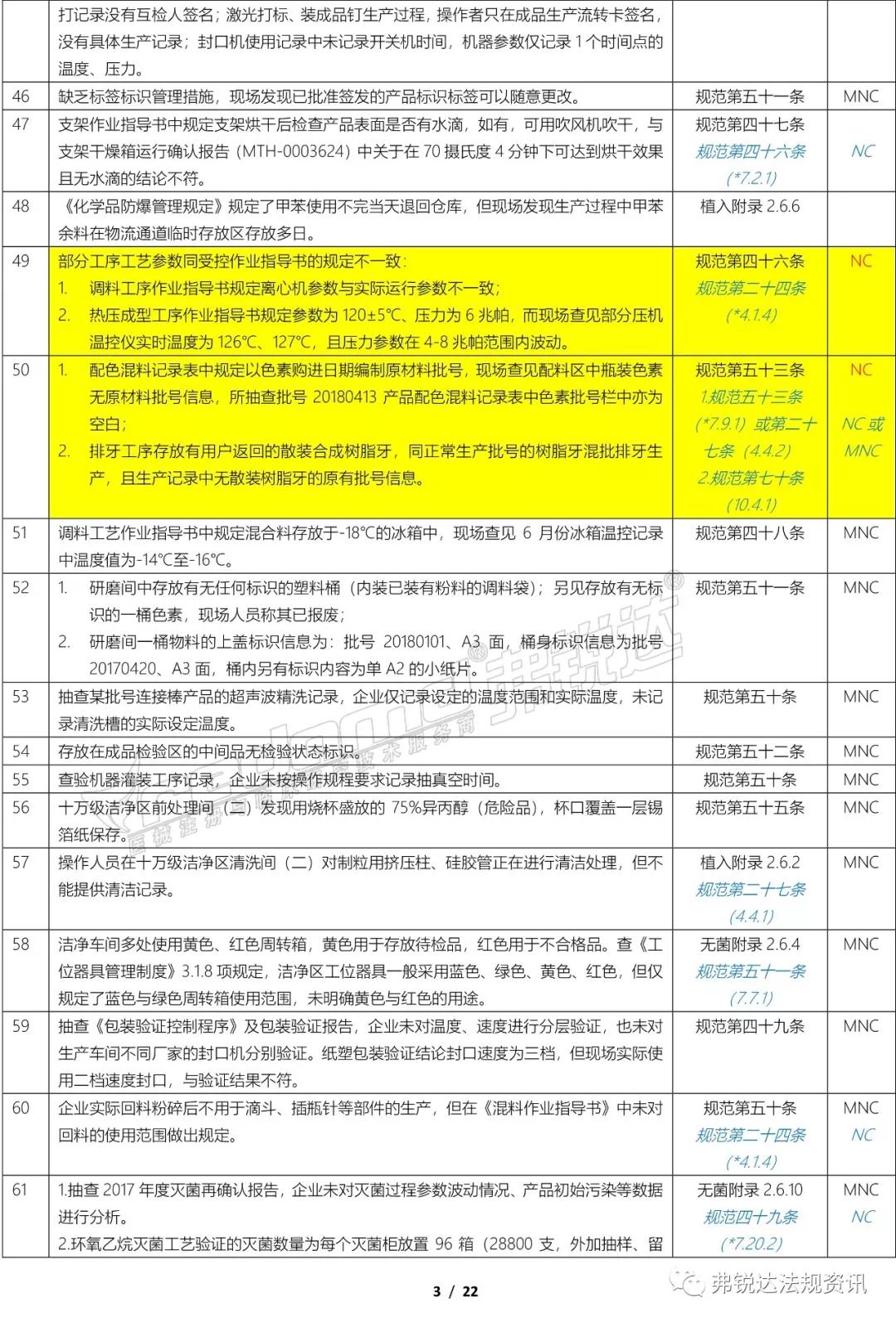
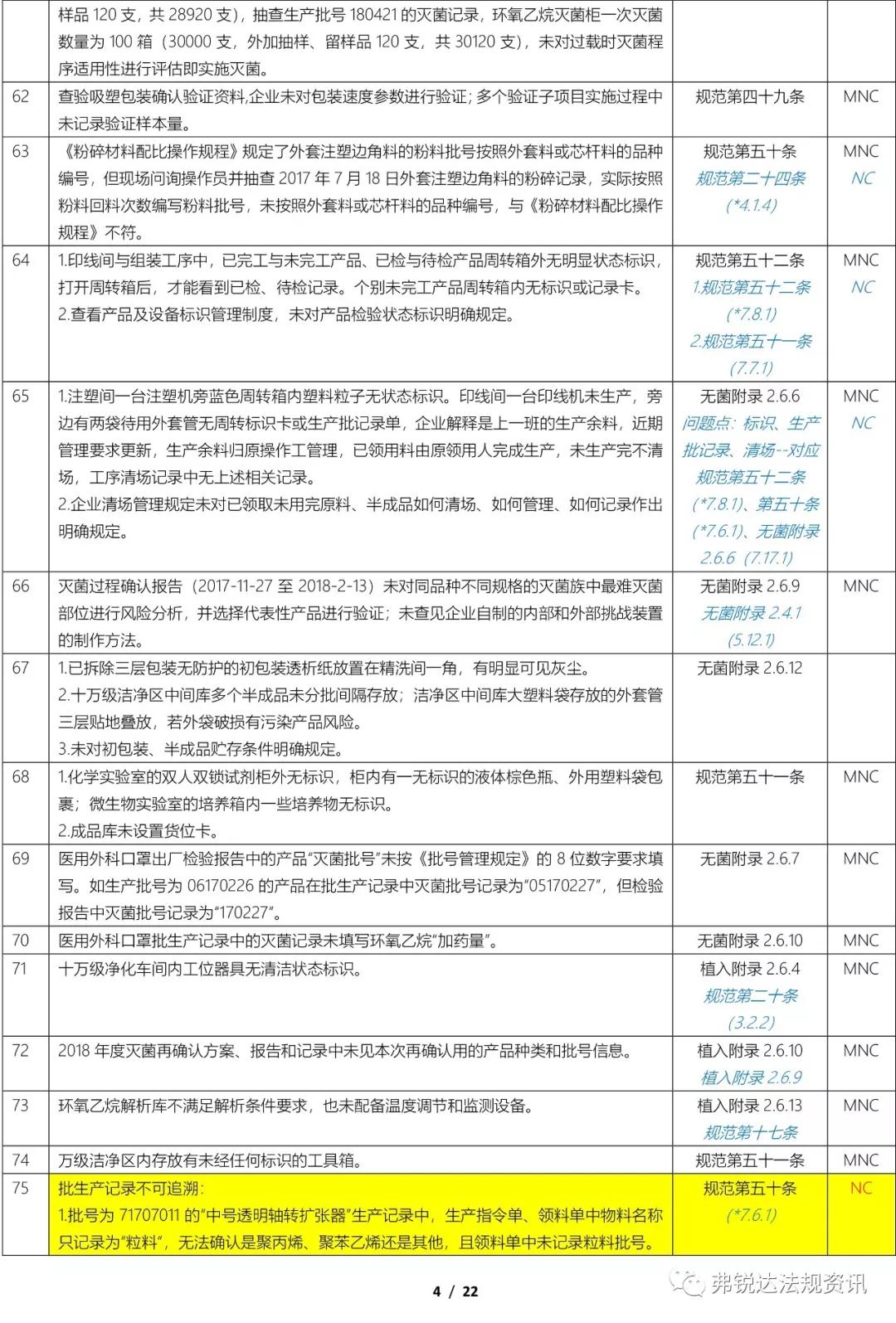
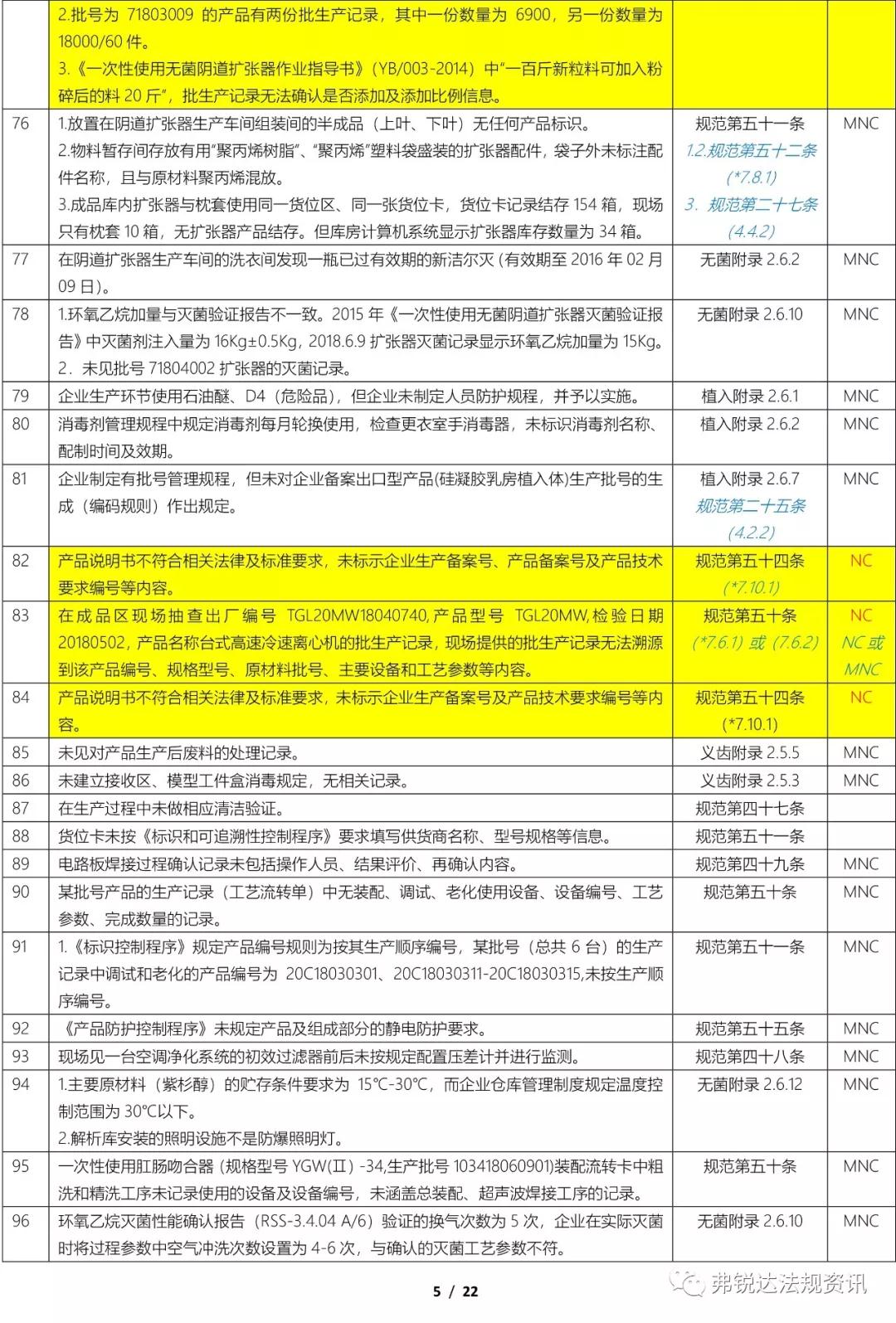
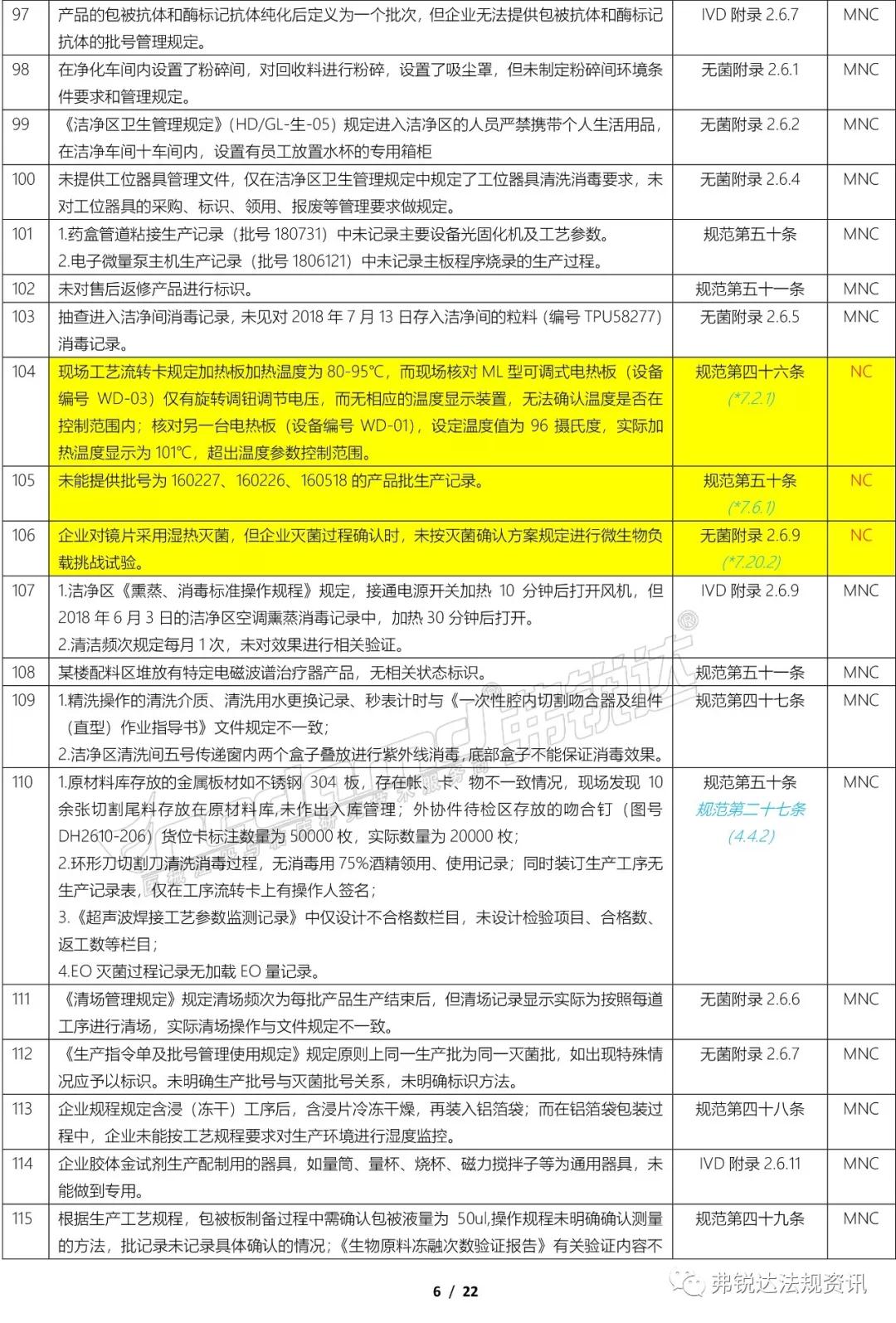
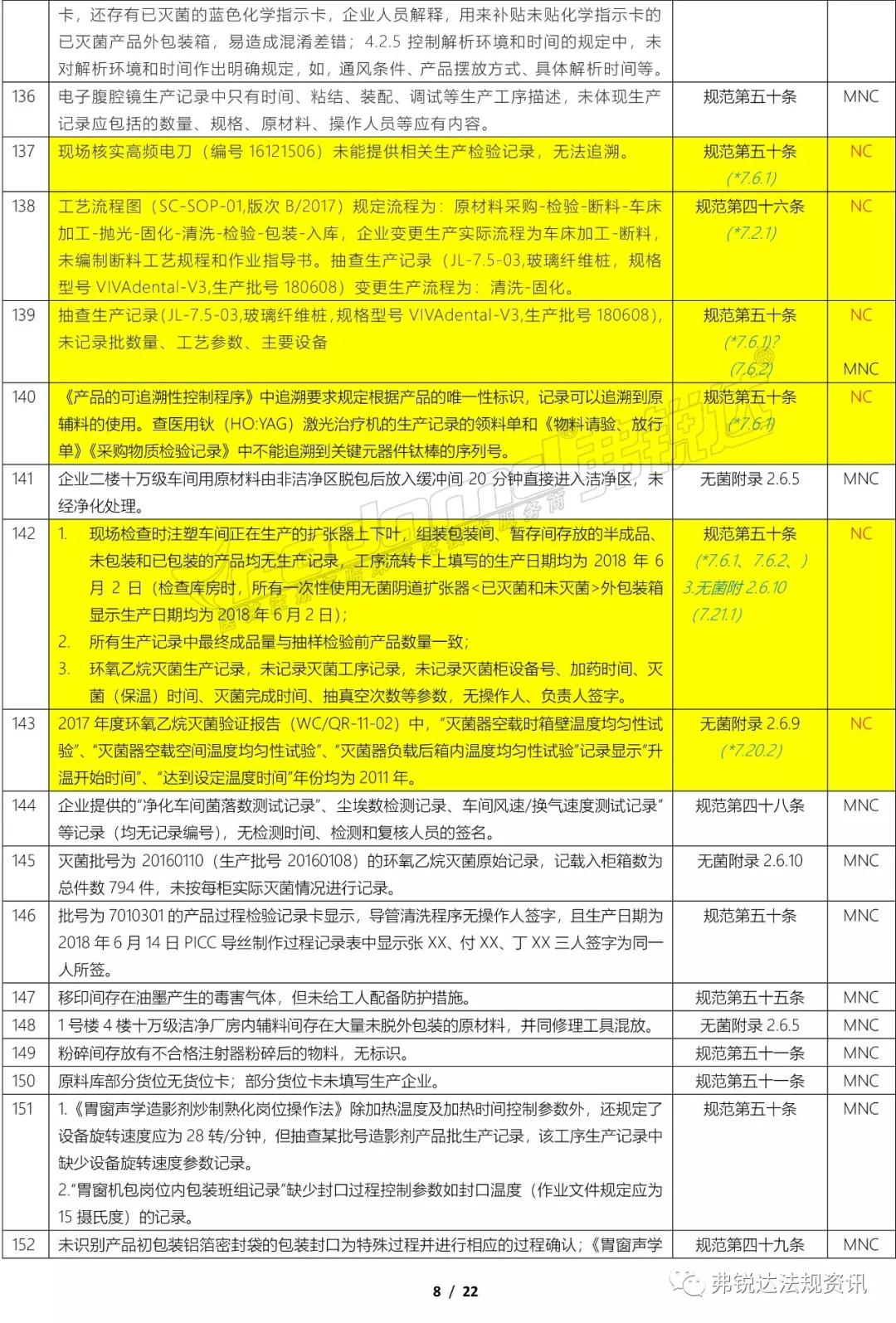
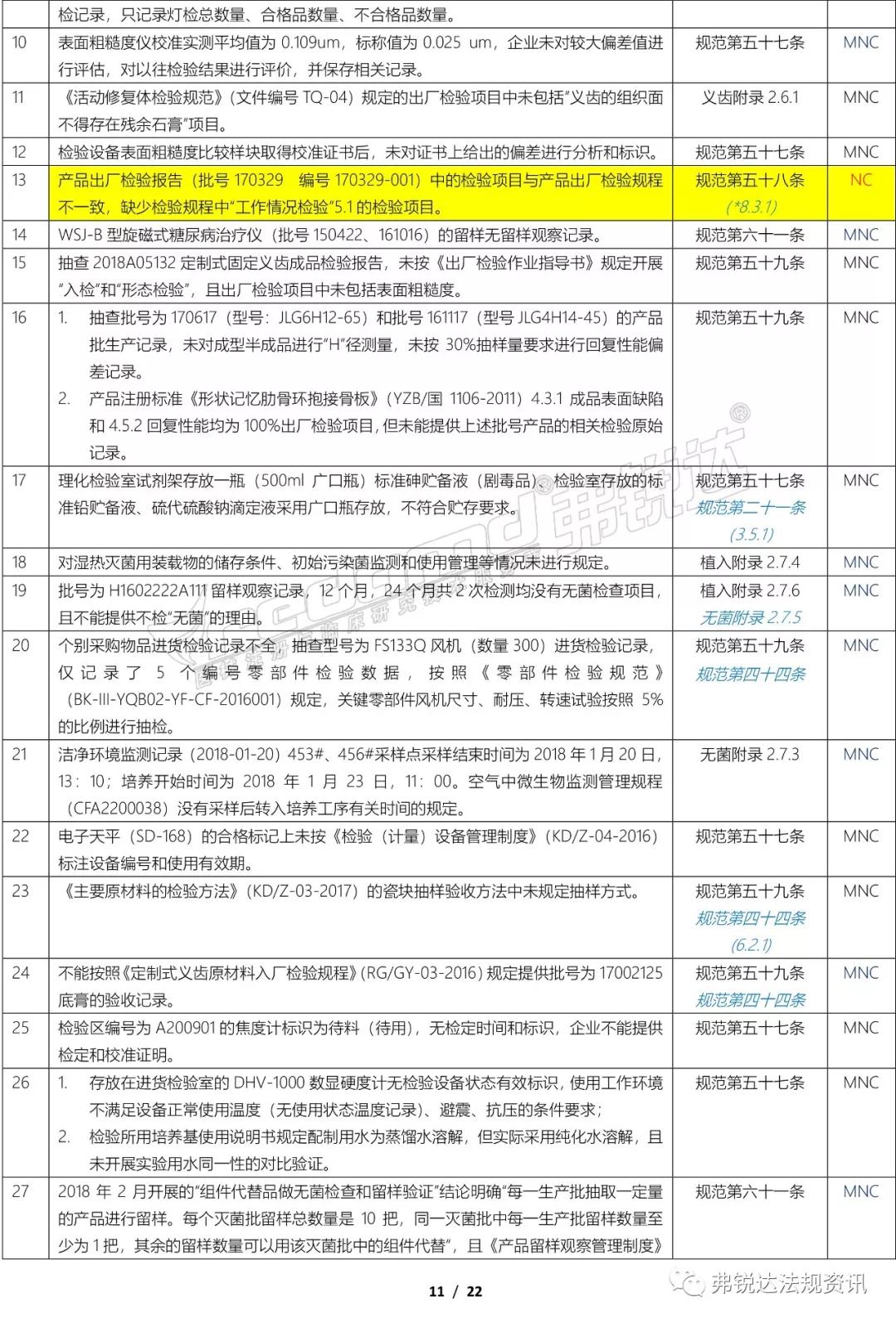
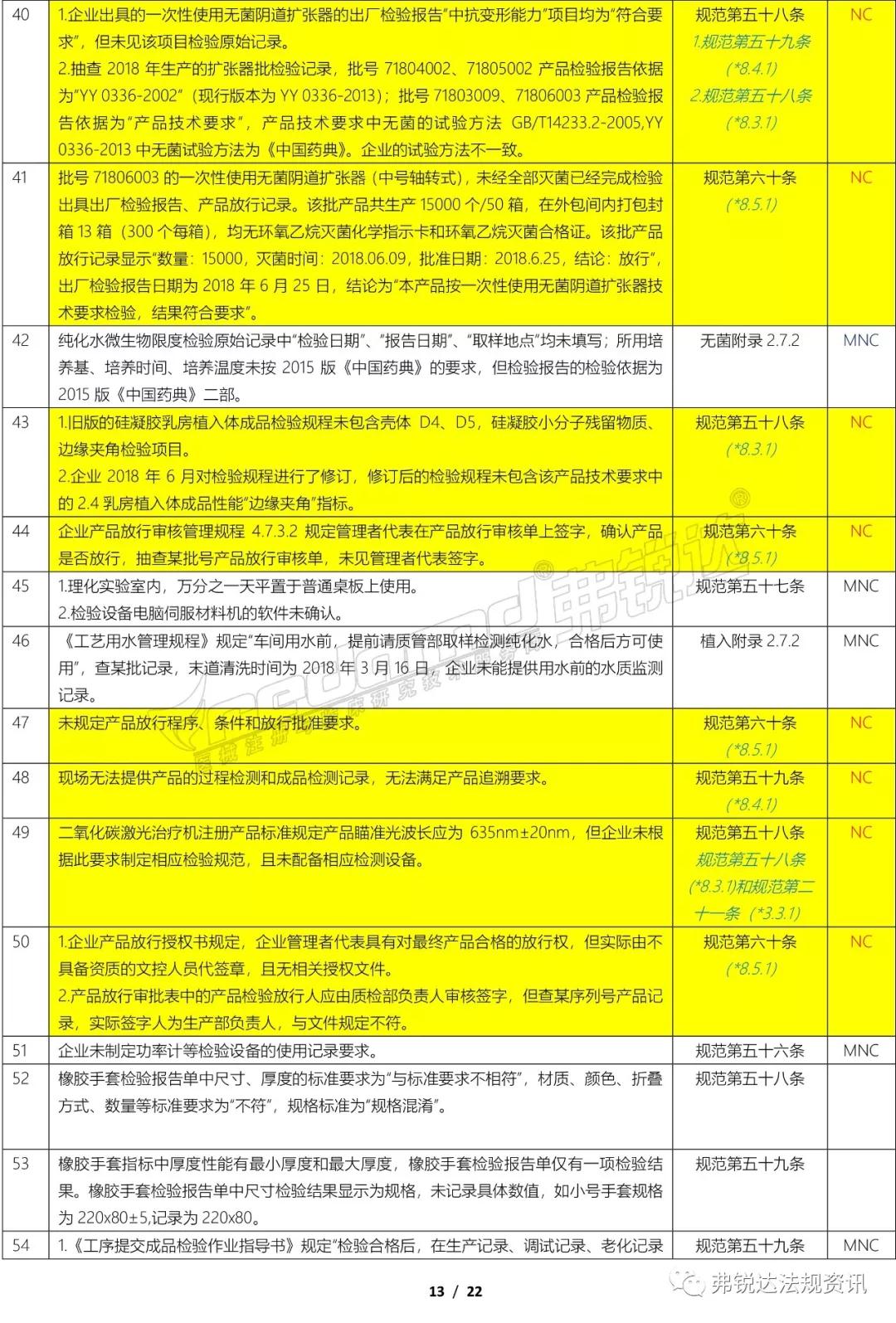
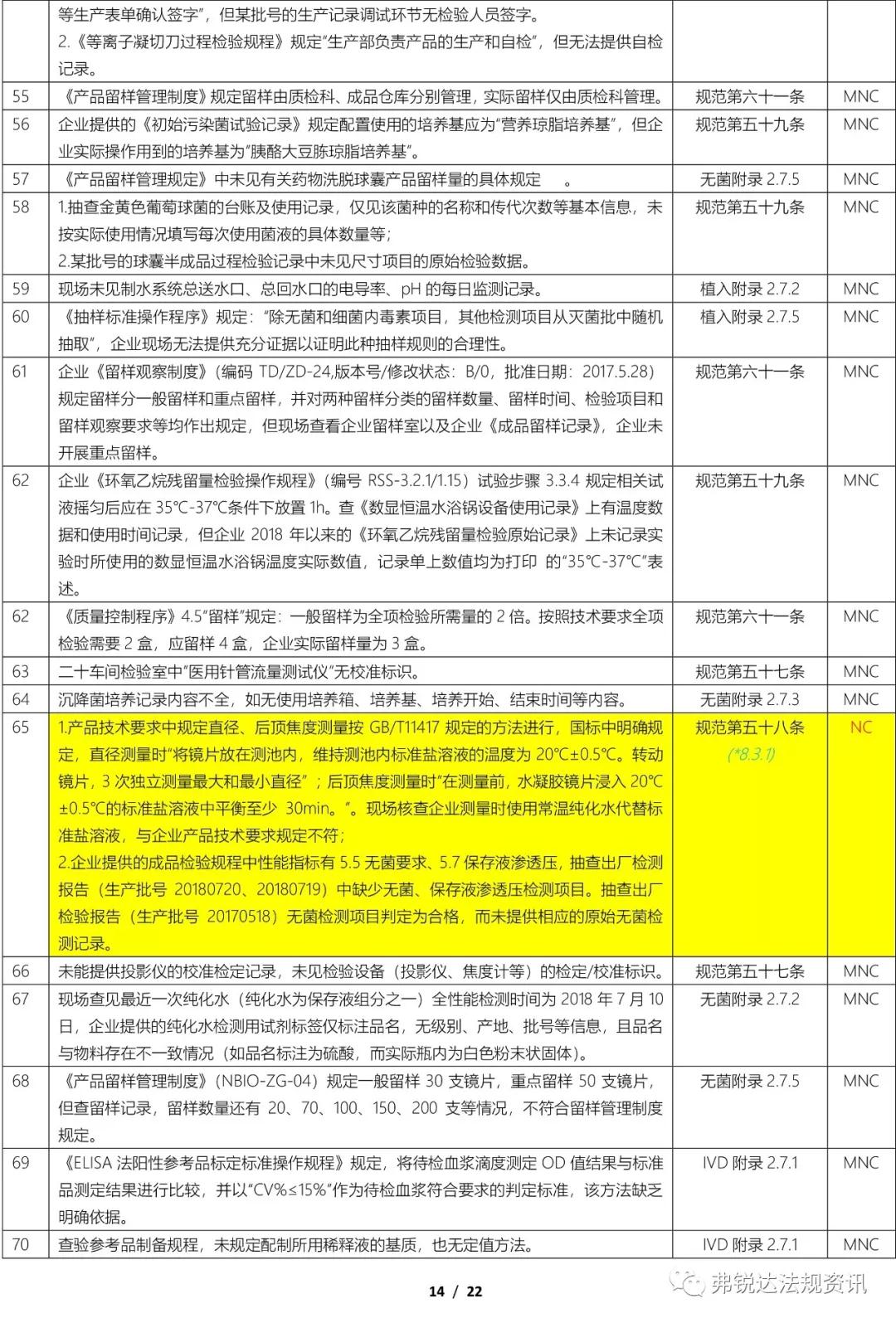
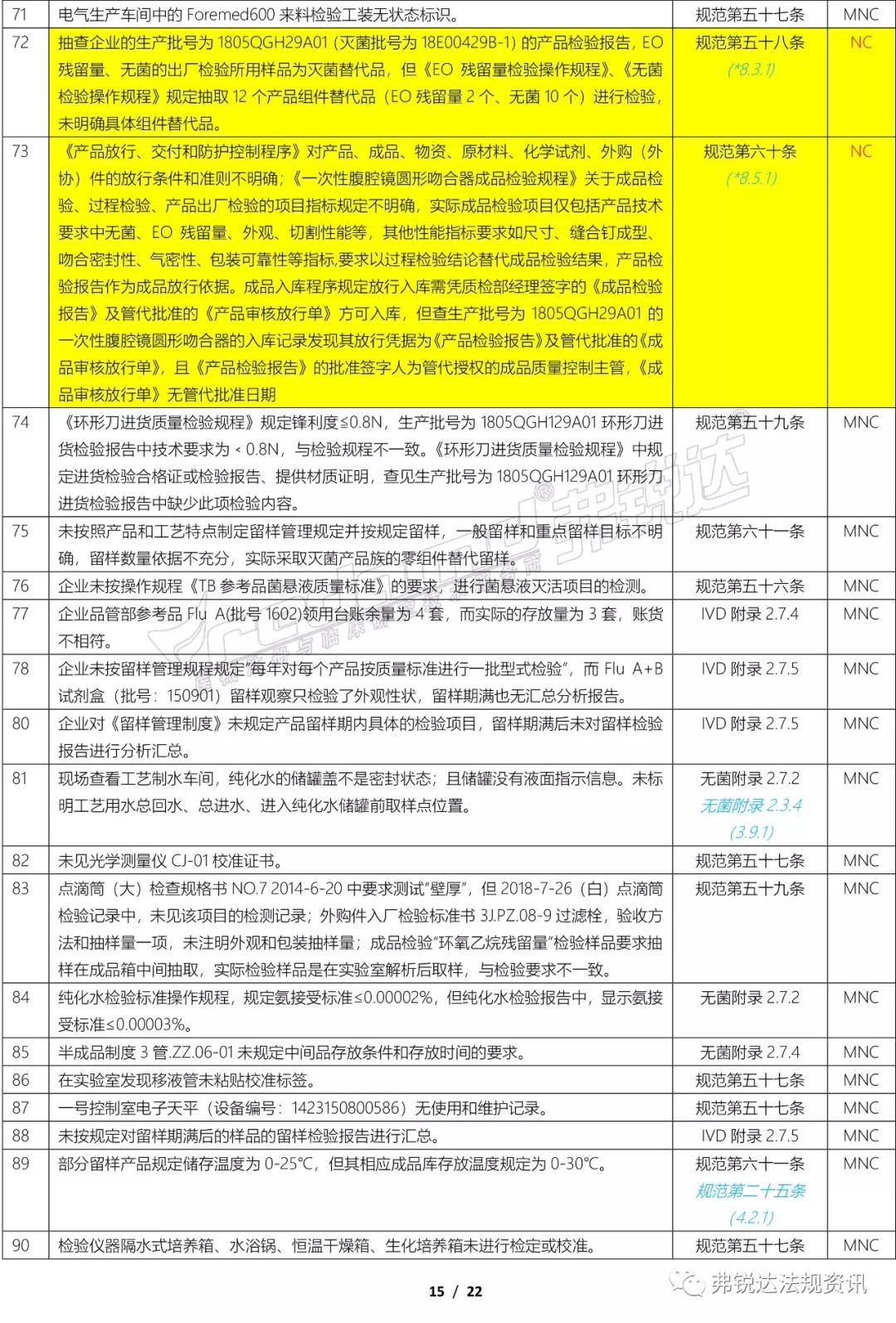
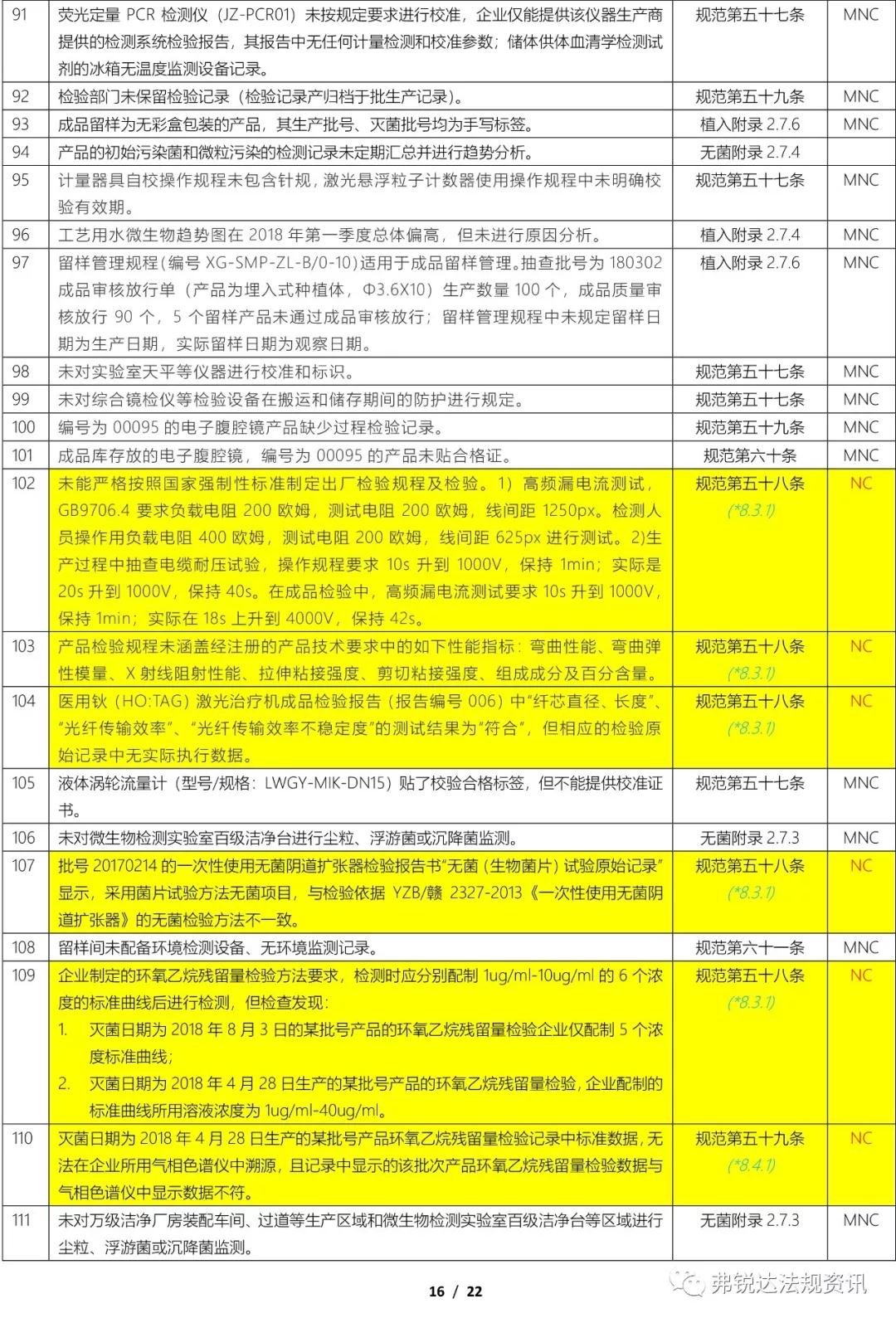
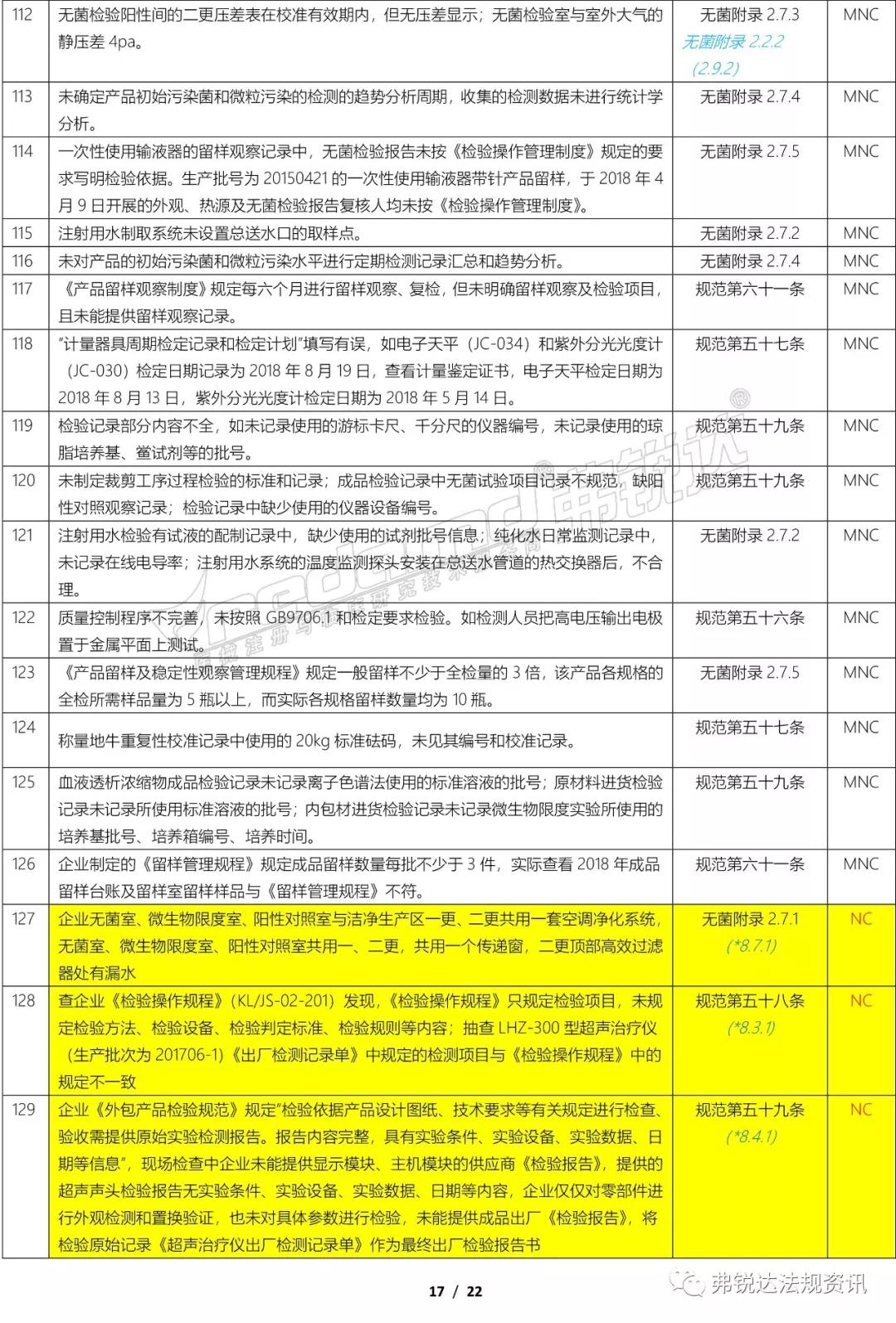
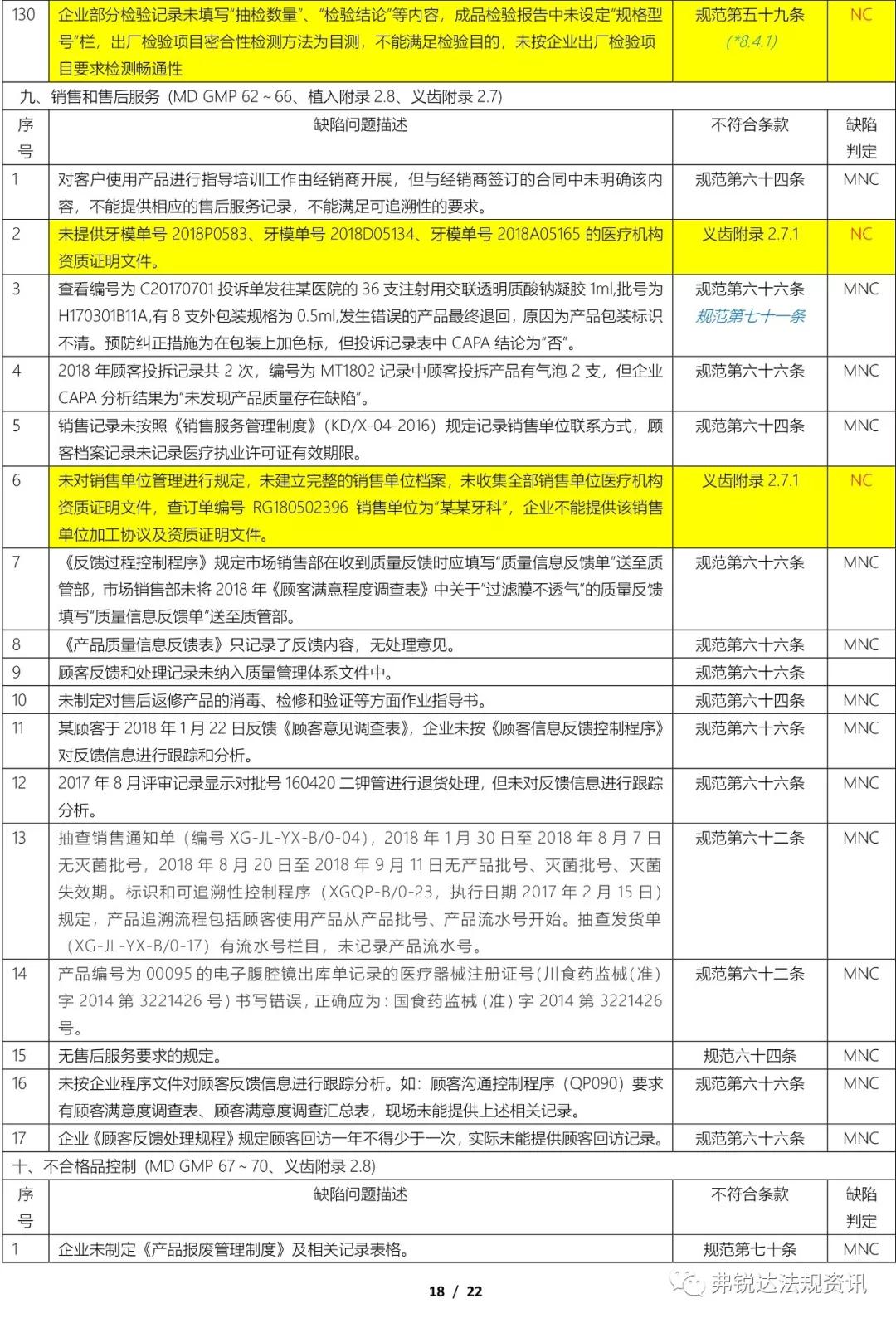
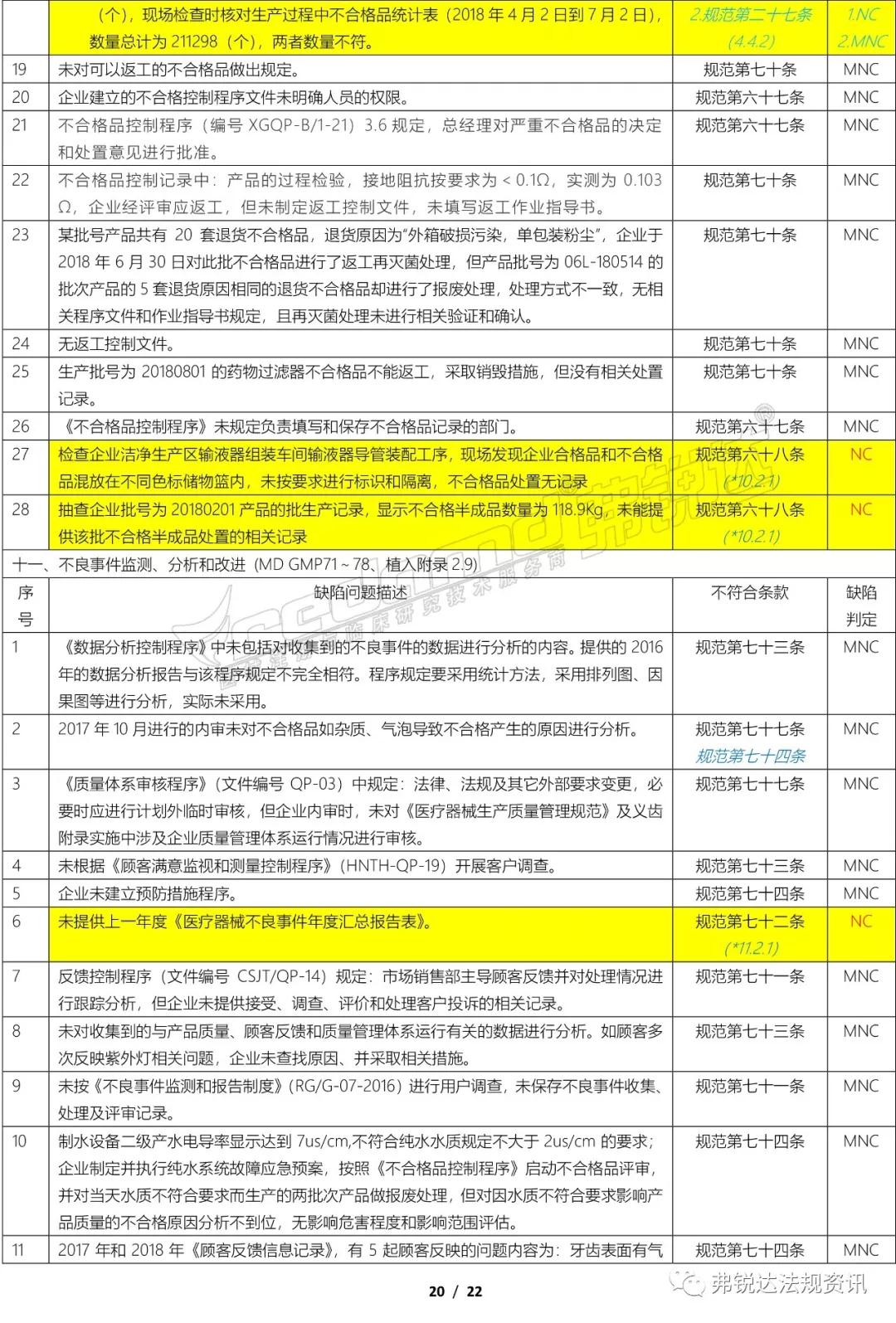
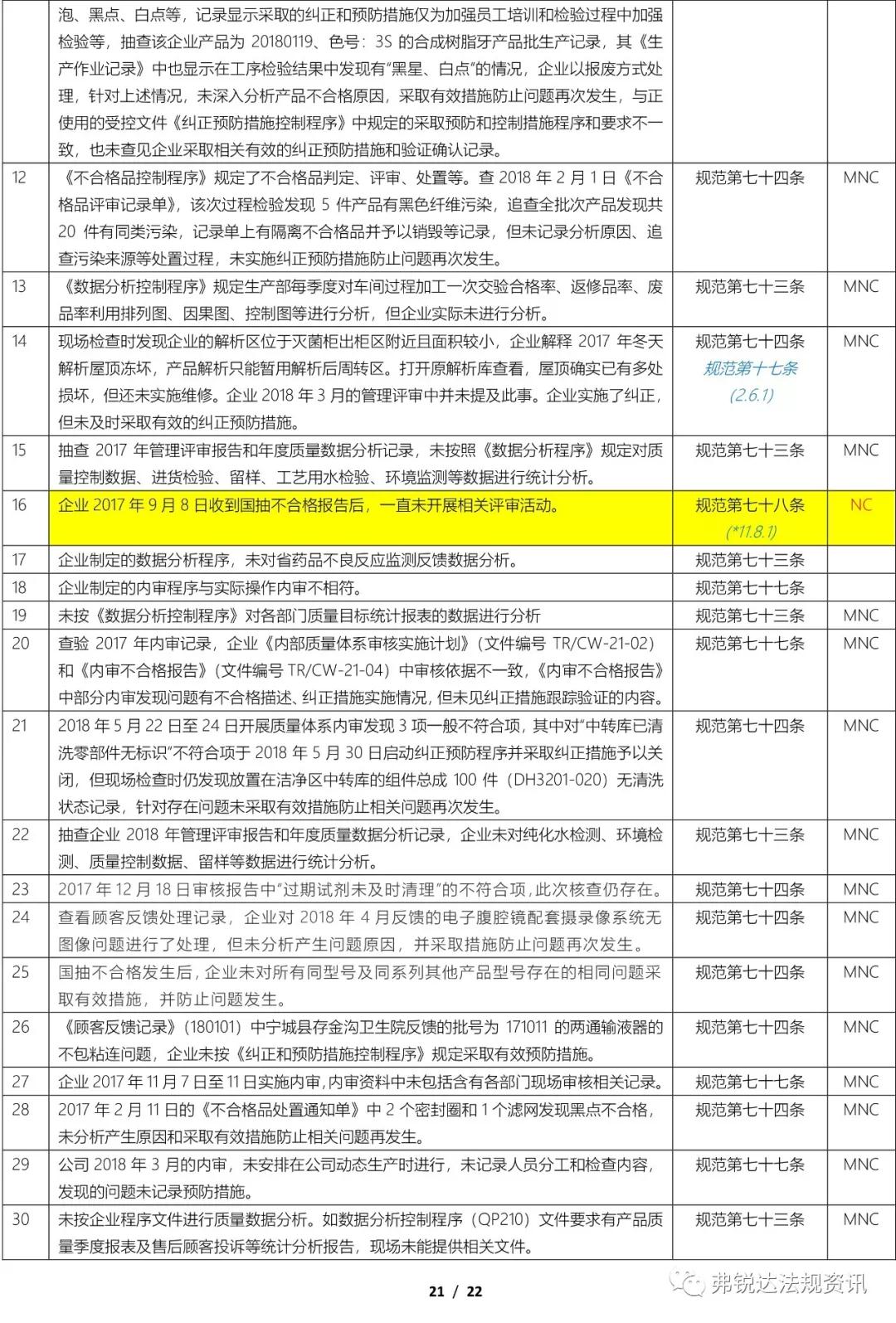
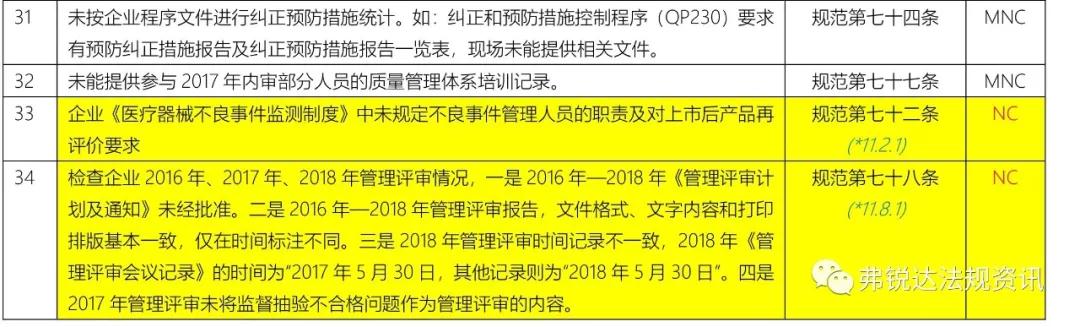
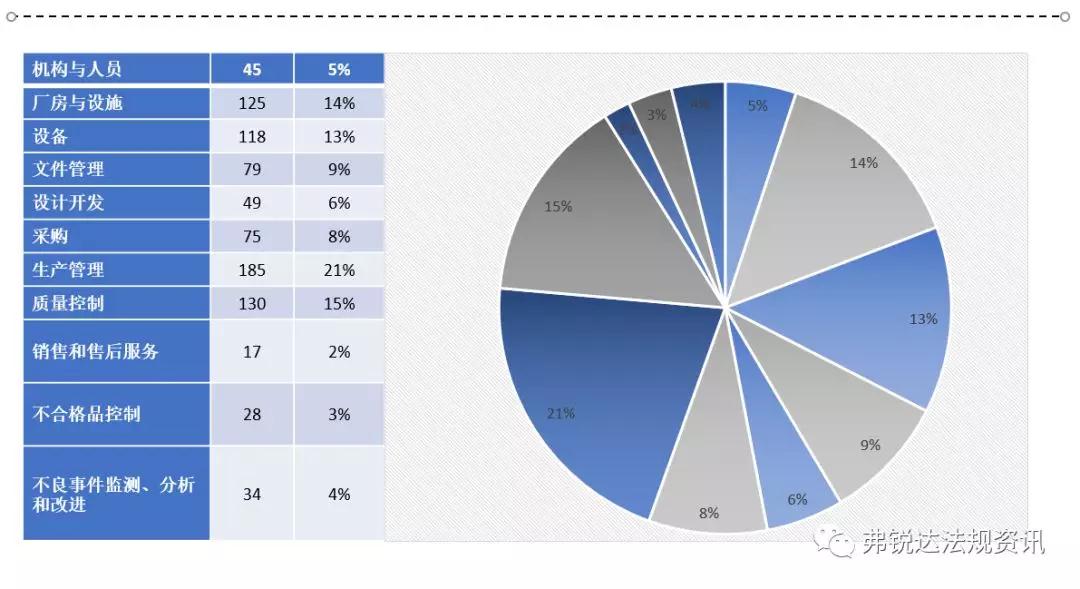
上篇: ①机构和人员(MD GMP 5~11、无菌附录2.1、植入附录2.1、IVD附录2.1、义齿附录2.1) ②厂房与设施(MD GMP 12~18、无菌附录2.2、植入附录2.2、IVD附录2.2、义齿附录2.2) ③设备(MD GMP 19~23、无菌附录2.3、植入附录2.3、IVD附录2.3、义齿附录2.3) ④文件管理(MD GMP 24~27) ⑤设计开发 (MD GMP 28~38、无菌附录2.4、植入附录2.4、IVD附录2.4) ⑥采购(MD GMP 39~44、无菌附录2.5、植入附录2.5、IVD附录2.5、义齿附录2.4) 下篇: ⑦生产管理(MD GMP 45~55、无菌附录2.6、植入附录2.6、IVD附录2.6、义齿附录2.5) ⑧质量控制(MD GMP 56~61、无菌附录2.7、植入附录2.7、IVD附录2.7、义齿附录2.6) ⑨销售和售后服务(MD GMP 62~66、植入附录2.8、义齿附录2.7) ⑩不合格品控制 (MD GMP 67~70、义齿附录2.8) ⑪不良事件监测、分析和改进(MD GMP71~78、植入附录2.9) (图片建议放大查看)▼ 上篇(①-⑥):2018年国家局飞检不合格项汇总分析(上篇) 2018年NMPA飞检缺陷分布统计 备注: 整理者:龙翔 1.原始资料来源于NMPA 官网或其它公开渠道所收集的2018年医疗器械飞行检查通报