10月1日起医械产品必须有身份证,这116家企业是急先锋
时间:2019-09-10 16:38发布者:厦门市医疗器械协会浏览量:1651
8月26日,国家药监局发布《医疗器械唯一标识系统规则》(以下简称《规则》)。《规则》共18条,明确了医疗器械唯一标识系统建设的目的、适用对象、建设原则、各方职责和有关要求,自2019年10月1日起正式施行。第一批参与唯一标识系统试点医疗器械企业,共116家。包括:上海微创医疗器械(集团)有限公司、山东威高集团医用高分子制品股份有限公司、深圳迈瑞生物医疗电子股份有限公司、乐普(北京)医疗器械股份有限公司、美敦力(上海)管理有限公司、碧迪医疗器械(上海)有限公司等。




医疗器械唯一标识(Unique Device Identification,简称UDI),是医疗器械产品的电子身份证,由产品标识和生产标识组成。产品标识是识别注册人/备案人、医疗器械型号规格和包装的唯一代码,是从数据库获取医疗器械相关信息的“关键字”,是唯一标识的必须部分;生产标识包括与生产过程相关的信息,包括产品批号、序列号、生产日期和失效日期等,可与产品标识联合使用,满足医疗器械流通和使用环节精细化识别和记录的需求。唯一性是首要原则,是确保产品精确识别的基础,是唯一标识发挥功能的核心原则。由于医疗器械产品的复杂性,唯一性应当与产品识别要求相一致,对于相同特征的医疗器械,唯一性应当指向单个规格型号产品;对于按照批次生产控制的产品,唯一性指向同批次产品;而对于采用序列号生产控制的医疗器械,唯一性应当指向单个产品。稳定性是指唯一标识一旦分配给医疗器械产品,只要其基本特征没有发生变化,产品标识就应该保持不变。当医疗器械停止销售、使用时,其产品标识不得用于其他医疗器械;重新销售、使用时,可使用原产品标识。可扩展性是指唯一标识应当与监管要求和实际应用不断发展相适应,“唯一”一词并不意味着对单个产品进行序列号化管理,在唯一标识中,生产标识可以和产品标识联合使用,实现规格型号、批次和单个产品三个层次的唯一性,从而满足当前和未来对医疗器械的识别需求。具体编码规则是,医保医用耗材编码分5个部分共20位,通过大写英文字母和阿拉伯数字按特定顺序排列表示。其中第一部分是耗材标识码,第二部分是分类码,第三部分是通用名码,第四部分是产品特征码,第五部分是生产企业。
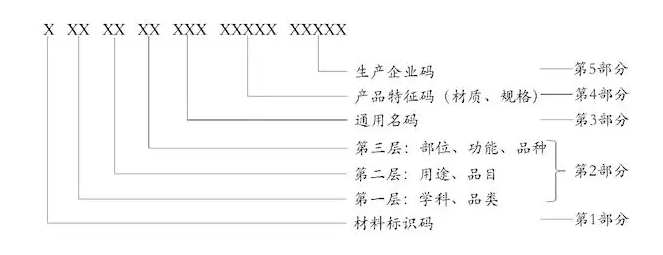
医疗器械唯一标识数据汇聚和共享通过医疗器械唯一标识数据库实现,该数据库由国家药品监督管理局组织建设,由注册人/备案人将唯一标识的产品标识及关联信息按照相关标准和规范上传至数据库,并对数据的准确性、唯一性负责。医疗器械经营企业、医疗机构、政府相关部门及公众可通过数据查询、下载、数据对接等方式共享唯一标识数据。
《规则》实施之日起,注册人/备案人应当在申请相关医疗器械注册、注册变更或者办理备案时,在注册/备案管理系统中提交其产品标识。相关医疗器械产品应当在生产过程中赋予医疗器械唯一标识,在产品上市销售前应当完成医疗器械唯一标识产品标识和相关数据的上传。《规则》实施之日前已生产、销售的医疗器械可不具备医疗器械唯一标识。
当前市面上常用的数据载体包括一维码、二维码和射频标签(RFID)。一维码是只在一维方向上表示信息的条码符号,应用多年已经很成熟,成本低,能很好兼容市面上现有的扫码设备,但一唯码所占空间大,破损纠错能力差。二维码是在二维方向上都表示信息的条码符号,相比于一维码,相同空间能够容纳更多的数据,在器械包装尺寸受限的时候能发挥很好的作用,具备一定的纠错能力,但对识读设备的要求相较于一维码要高。射频标签具有信息存储功能,能接收读写器的电磁调制信号,并返回相应信号的数据载体。射频标签的载体成本和识读设备成本相较于一维码和二维码要高,但RFID读取速度快,可以实现批量读取,在某些环节和领域能够发挥作用。注册人/备案人可根据产品的特征、价值、主要应用场景等因素选择适当的医疗器械唯一标识数据载体。器械唯一标识的发码机构应当为中国境内的法人机构,具备完善的管理制度和运行体系,确保按照其标准创建的医疗器械唯一标识的唯一性,并符合我国数据安全有关要求。发码机构应当向注册人/备案人提供执行其标准的流程并指导实施,为便于注册人/备案人等掌握发码机构的编码标准,供相关方选择或应用,发码机构应当将其编码标准上传至医疗器械唯一标识数据库并动态维护。每年1月31日前,发码机构应当向国家药品监督管理局提交按照其标准创建的唯一标识上一年度的报告。第一步:注册人/备案人按照《规则》和相关标准,结合企业实际情况选择发码机构。第二步:注册人/备案人按照发码机构的标准创建产品标识,并确定该产品生产标识的组成。第三步:《规则》实施之日起,申请医疗器械注册、注册变更或者办理备案的,注册人/备案人应当在注册/备案管理系统中提交产品标识。第四步:注册人/备案人根据发码机构标准选择适当的数据载体,对医疗器械最小销售单元和更高级别的包装或医疗器械产品上赋予医疗器械唯一标识数据载体。第五步:注册人/备案人在产品上市销售前将产品标识和相关信息上传至医疗器械唯一标识数据库。第六步:产品标识及数据相关信息变化时,注册人/备案人及时更新医疗器械唯一标识数据库。
(资料来源:国家药监局官网)







