前 言
近年来,国家对医疗器械生产企业的生产质量管理体系的监管管理力度逐渐加强,2015年5月18日,国家食品药品监督管理总局局务会议审议通过《药品医疗器械飞行检查办法》,且于2015年9月1日正式施行。
自2018年5月9日起,根据国家局网站公布的内容,国家局共对全国91家医疗器械生产企业进行了飞行检查,其中已经停产的企业为20家,即实查企业为71家。
首先,我们对71家生产企业飞行检查不合格项目所出现在《医疗器械生产质量管理规范》的相应章节分布进行统计。
图一:
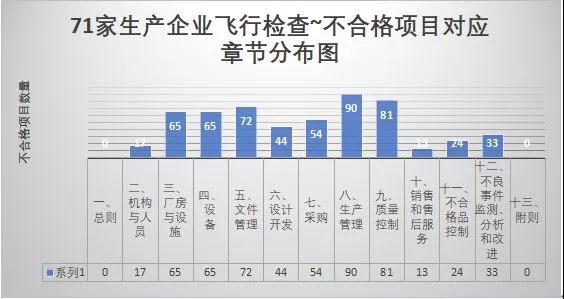
其次,结合《医疗器械生产质量管理规范》的要求,我们对如上71家生产企业飞检问题所占比例进行分类如下:
图二
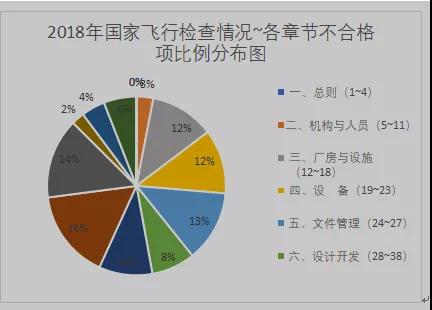
另外,按照《医疗器械生产质量管理规范》的具体条款要求,对这71家生产企业出现不合格项目的次数进行统计如下:
图三
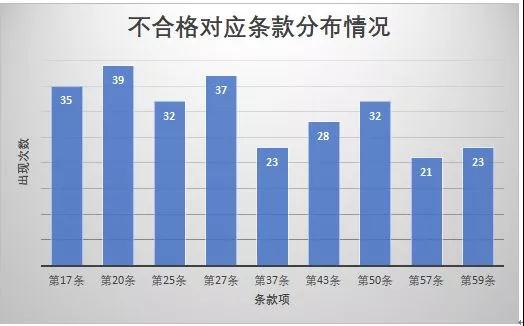
同时,结合71家生产企业实际问题,在相应条款上具体问题主要体现如下表:

最后,我们结合《医疗器械生产质量管理规范》,对这71家生产企业的飞行检查情况具体问题进行汇总如下:
1-4无不合格项目,未在下表中体现





【来源】周美琴 医疗器械注册与临床